
武汉科技大学最新科研进展!
日期:2026-03-23 09:48
阳春三月,武汉科技大学在多个领域发表重要学术成果。
1.计算机科学与技术学院在国际顶级期刊发表重要研究成果
近日,计算机科学与技术学院青年教师王海云博士在空间多组学数据分析研究领域取得重要进展,相关成果“SpaDDM: Integrating Spatial Multi-omics with Directional Graph Diffusion Models to Dissect Spatial Patterning and Signaling”,被国际顶尖综合性学术期刊 《PNAS》接收,武汉科技大学为第一单位,王海云为第一作者。
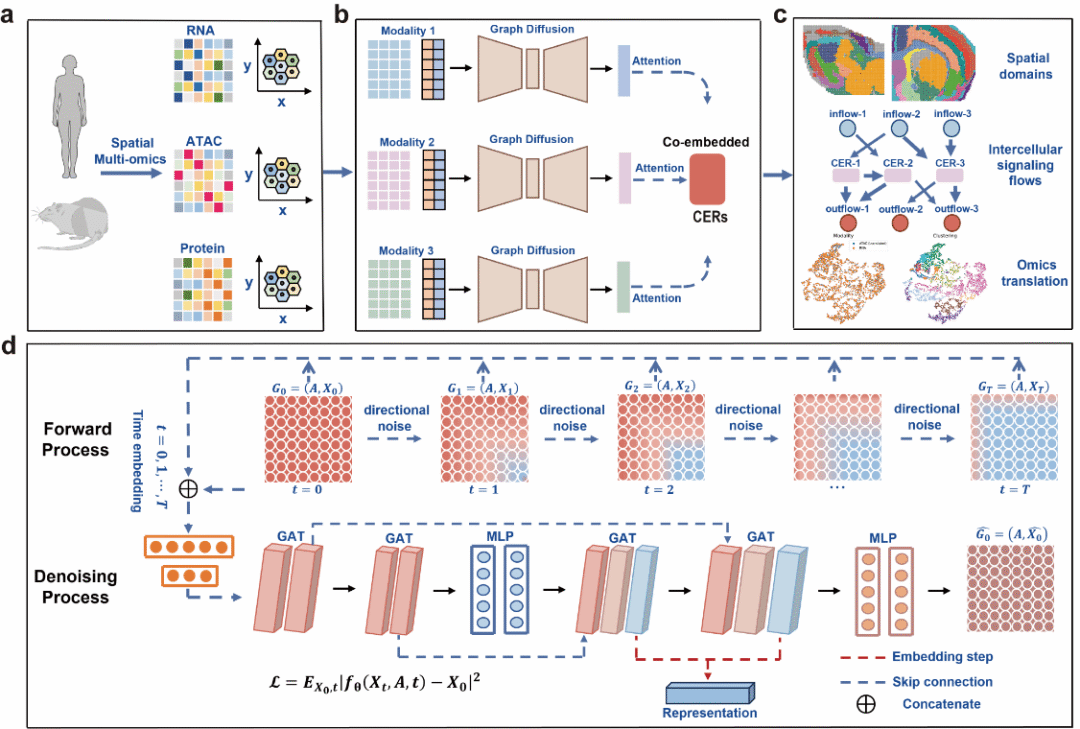
研究团队提出了一种基于有向扩散模型的空间多组学整合框架 SpaDDM(图1)。针对空间多组学中的各向异性特征,SpaDDM 引入数据依赖的方向性噪声建模,增强对组织结构与空间边界的刻画能力,提升区域分割精度与稳定性。模型以空间感知的共嵌入低维表征(CERs)为媒介,整合多组学信息,结合 COMMOT 与 CellChatDB 推断配体—受体作用,并整合 GLUE 与 snapATAC2 鉴定关键转录因子,构建“流入信号→CER→转录因子→流出信号”的多层级信号网络,实现细胞通讯的多组学整合解析。
该研究为空间多组学数据的统一建模与生物学解释提供了一种高效而通用的计算框架,不仅加深了对组织异质性和空间信号调控机制的理解,也为发育生物学、组织微环境研究及疾病机制解析提供了重要工具和新思路。
2.医学部田波团队联合华科大张培团队发表社交行为调控神经机制重要研究成果
近日,医学部田波团队与华中科技大学同济医学院张培团队在PNAS杂志在线发表了题为“Divergent BLA engram circuits orchestrate social preference dynamics in bystander male mice with self-experienced stress”的研究论文,揭示了源自基底外侧杏仁核(BLA)印迹细胞的神经环路调控社交偏好和社交回避行为的核心机制。
个体自身经历对其社交选择的灵活性具有重要调控作用,该现象背后蕴含着趋利避害的生物进化本质。社交灵活性不仅是个体塑造健康心理状态、实现心理适应的重要过程,更是社会关系得以建立、发展与维持的核心环节。以往研究已证实,个体先前的社交相关自身经历,会对社交认知、社交偏好及社交回避等各类社会行为产生重大影响。然而,先前社交经历的相关信息如何转化为后期适应性社交行为的神经机制尚不清楚。

大量研究表明,基底外侧杏仁核(basolateral amygdala,BLA)在社交失败应激相关创伤记忆的储存、再巩固和提取中发挥重要的作用。课题组前期也证实了社交失败创伤记忆由BLA印迹细胞(BLA engram cells,BLAEC)存储与编码(Neuron,2024)。“记忆印记细胞”(Engram cells)的科学概念最早由Richard Semon于1904年提出,将机体事件经历在神经系统中留下的持久物理与化学改变命名为记忆印迹(Engram),认为特定神经元群被经验激活并发生可塑性修饰后,可在后续线索触发下重新激活以实现记忆提取。因此,作者推测BLA记忆印记细胞可能参与驱动具有社交失败经历个体的后续社交灵活性,包括社交偏好和社交回避行为。
该研究聚焦社交失败经历调控后续社交选择的神经机制这一科学问题,建立联合单次社交失败应激(SSDS)和替代性社交失败应激(VSDS)的小鼠模型,综合运用光遗传学、病毒示踪、在体电生理记录、光纤钙成像等前沿技术开展研究。研究发现,SSDS相关BLA印迹细胞是调控小鼠社交行为动态变化的关键,其与前扣带回皮层谷氨酸能神经元形成的BLA EC-ACC环路,是介导社交行为改变的核心环路;而该环路下游的BLA-ACC-dHPC、BLA-ACC-vHPC、BLA-ACC-ZI 三条分支,分别特异性调控社交偏好、社交回避,以及两种行为的共同调控。
研究从 “记忆印记细胞” 的独特视角,首次明确了早期社交失败经历驱动社交行为灵活性的神经环路机制,填补了先前社交经历转化为适应性社交行为神经机制的研究空白,进一步加深了学界对社交行为本质及社交障碍相关脑疾病发生机制的理解,为抑郁症、创伤后应激障碍(PTSD)等与社交行为异常相关疾病的机制研究和干预策略开发提供了全新的理论依据和研究靶点。研究同时指出,样本仅局限于雄性小鼠、ACC 神经元群体下游投射的空间分布差异尚未解析为当前研究局限性,为后续研究指明了方向。
3.医学部曾燕/李金泉团队揭示肝-脑轴介导臭氧暴露所致认知缺陷
近日,医学部的曾燕/李金泉团队在Journal of Neuroinflammation上发表了题为“Ozone-induced cognitive deficits are mediated by the liver-brain axis: peripheral complement C3 triggers microglial synaptic phagocytosis”的文章。第一作者为王友刚博士,通讯作者为李金泉教授和曾燕教授。此项研究揭示了臭氧导致认知损伤的一条全新通路——肝-脑轴。

该研究发现,臭氧暴露首先引起肝脏损伤与补体C3的释放,随后外周C3转移至大脑,促使小胶质细胞对海马突触进行异常“修剪”,从而损害认知功能。这一结论强调了肝脏在中枢神经毒性中的关键介导作用,将臭氧神经毒性的研究视角从传统的中枢层面拓展至外周器官互作层面,对未来的神经毒理学研究、相关疾病防治及环境健康风险评估具有重要的启示意义。
研究通过动物实验与多组学分析,首次揭示了肝源性补体C3在臭氧神经毒性中的关键介导作用。臭氧暴露激活肝脏补体系统,促使C3释放入血,并在血脑屏障受损后进入海马区,通过C3/CR3轴激活小胶质细胞,导致其过度吞噬兴奋性突触,最终引发认知缺陷。这一发现确立了“肝-脑轴”作为臭氧神经毒性的核心通路,将研究视角从传统的中枢氧化应激拓展至系统性器官间通讯。值得注意的是,臭氧诱导的补体激活呈现C3依赖性但非C1q依赖性,且海马区C3升高源于肝脏而非局部合成。肝脏特异性C3敲低可同时逆转外周及中枢C3水平、小胶质细胞活化、突触损伤及认知缺陷,为靶向干预提供了理论依据。本研究的局限性包括:米诺环素的非特异性作用需通过小胶质细胞特异性遗传模型进一步验证;循环C3穿越受损血脑屏障的直接证据仍需确证。未来研究应聚焦于肝脏C3表达与小胶质细胞活化的动态时序关系,并探索外周C3作为神经毒性生物标志物的临床潜力。
4.电子信息学院在《Nature Communications》发表重要研究成果
近日,电子信息学院万达副教授团队与湖南大学半导体学院廖蕾教授团队合作,在《Nature Communications》发表了题为“High-speed energy-efficient memristor confined in sub-5 nm space with elemental oxygen reservoir layer”的论文。武科大2021级硕士生李晨飞为论文第一作者,万达副教授为论文通讯作者,武科大为论文第一完成单位。

忆阻器凭借可调电阻、非易失性、存算一体化的独特特性,成为突破传统冯诺·依曼架构瓶颈、推动集成电路向存算一体方向演进的核心候选器件,也是当前集成电路领域的前沿研究热点。该论文研制的新型忆阻器,精准对标集成电路先进制程与低功耗应用需求,创新性采用MoS2/HfOX/EOR/HfS2垂直异质结构,将3.5 nm元素氧储存层精准限域于亚5 nm的微纳空间内。该器件依托二维材料原子级的平整界面,实现了电场的均匀分布,通过电场精准调控氧空位的定向迁移与复合,达成电阻状态的高精度切换;同时,元素氧储存层兼具氧空位扩散屏障的功能,与HfOₓ隧穿层协同构建起双重限流结构,既有效解决了传统超薄器件漏电流过大的行业难题,又保障了阻变过程的高可控性与高一致性。
该新型忆阻器具备微缩性优异、功耗低、可实现存算一体的核心优势,在高密度非易失性存储器、存算一体芯片、边缘计算芯片及物联网芯片等领域拥有广阔的应用前景。该器件可与CMOS工艺高度兼容并实现异质集成,将为芯片向更高集成度、更低功耗、更强算力的方向发展提供重要支撑。
新闻来源 | 武汉科技大学